바코드 있는 임상시험용약, 일반 약제와 동일적용
오는 10월20일부터는 견본품 등도 공급받은 자 명칭(공급처)과 사업자번호 정보를 공급내역 보고 시 반드시 기재해야 한다.
또 견본품 공급일자는 '제공일자'에서 '출하(공급)일자'로 변경되고, 바코드 확인이 가능한 임상시험용 의약품도 다른 의약품과 동일하게 공급내역을 보고한다.
건강보험심사평가원 의약품관리종합정보센터는 이 같이 '공급내역 보고기준 개선사항'을 8일 안내하고, 10월20일부터 적용한다고 밝혔다.
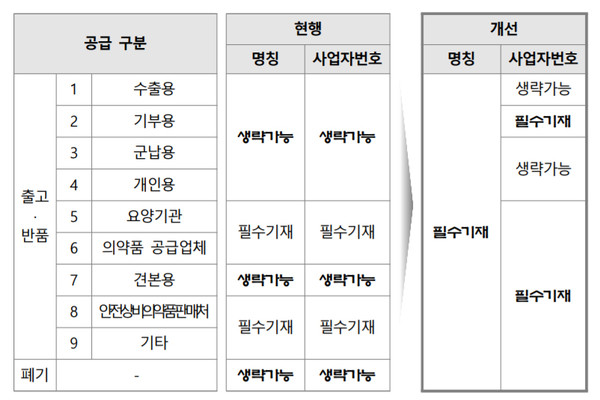
먼저 모든 의약품은 원칙적으로 출고, 반품, 폐기 시 공급받은 자 명칭과 사업자번호 정보를 기재하도록 변경된다. 현재는 요양기관, 의약품공급업체, 안전상비의약품판매처, 기타 등은 공급받은자 명칭과 사업자번호를 필수 기재하고, 수출용·기부용·군납용·개인용·견본용은 생략할 수 있도록 돼 있다. 폐기 때도 생략 가능하다.
앞으로는 공급받은 자 명칭은 모두 필수기재로 바뀐다. 단, 해외 기부·견본품 제공 등으로 기부·견본 보고 시 사업자번호를 기재할 수 없는 경우에는 사업자번호를 생략할 수 있다. 이 경우 비고란에 미기재 사유(해외기부 등)를 기재해야 한다.

견본품 공급일자도 변경된다. 견본품은 견본 제공을 목적으로 생산돼 포장에 '견본품' 혹은 'SAMPLE' 등 견본품이라는 식별가능한 표기가 있는 제품을 의미한다.
견본품의 공급일자는 현재 제공일자로 기재하고, 보고기한은 전문의약품의 경우 제공일 기준 익일, 일반의약품은 제공일 기준 익월로 돼 있다.
앞으로는 공급일자가 출하(공급)일자로 바뀌고, 보고기한도 제공일 기준이 아닌 출하일 기준으로 변경된다.

임상시험용 의약품 공급기준도 바코드 확인 불가 의약품과 가능 의약품으로 나눠 따로 적용된다. 바코드 확인 불가 의약품은 현재처럼 공급일자를 의약품 출하(공급)일자로 기재하고, 보고기한은 출하일 기준 익월로 한다. 제조번호, 유효기간, 일련번호는 생략 가능하다. 다만 비고란 기재방식은 'ZA/임상시험'에서 'ZA/식약처 승인번호'로 바뀐다.
바코드가 확인 가능한 임상시험용 의약품은 다른 의약품 공급내역 보고기준 및 방법을 그대로 적용받는다. 공급일자를 의약품 출하(공급)일자로 적고, 전문의약품 출하일 익일-일반의약품 출하익 익월에 보고한다. 또 전문의약품인 경우 제조번호, 유효기간, 일련번호를 생략할 수 없다.



